Elektrolit
İçinde saf su bulunan bir kaba iki elektrot daldırıp bu elektrotlar bir akünün kutuplarına bağlandığında akım devresinde bulunan ampermetrede hiç bir sapma görülmeyecektir. Yani akım akmayacaktır. Ancak su içine birkaç damla tuz ruhu damlatıldığında akım geçecek ve elektrotlardan kabarcıklar yükselecektir. Buradan çıkarılacak sonuç saf suyun yalıtkan olduğu buna karşın içine atılan asit ile iletken özellik kazanması ve akım geçişi esnasında kimyasal bir dönüşüm oluşmasıdır. Aynı sonuç asit yerine baz ya da tuz konulduğunda da gerçekleşir. Saf suya iletken özelliği kazandıran bu sıvılara ve bu sıvıları ayrıştırma olayına aşağıda detayı verileceği üzere sırasıyla elektrolit ve elektroliz ismi verilir.
Seyreltilmiş asitler bazlar çözünmüş ya da ergimiş tuzlar elektrik akımını geçirirler. İşte bu cins elektrik akımını geçiren sıvılar elektrolit olarak tanımlanır.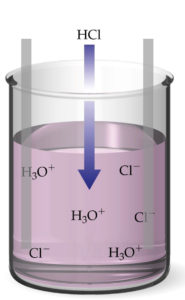
Asit molekülleri su içinde hareketli ve elektrik yüklü parçacıklara ayrışırlar. Bu yüklü parçacıklar iyon diye isimlendirilir. Örneğin suya katılan tuz ruhu su içinde pozitif yüklü hidrojen iyonları ( H+ ) ve negatif yüklü klor iyonlarına ( Cl– ) ayrışmıştır. Pozitif yüklü hidrojen iyonu bir elektron kaybetmiş hidrojen protonudur diye tanınır ancak gerçekte bu proton bir su molekülü ile birleşerek bir hidroniyum iyonu( H3O+ ) oluşturmuştur.
Hidrojen iyonları ve metal iyonları daima pozitif yüklüdür. Asit ve baz kökleri ise negatif iyonları oluşturur.
Elektroliz
Şekildeki elektrotlara bir doğru akım uygulandığında, kabın içinde bir iyon hareketi başlar. Negatif yüklü iyonlar pozitif elektrota (anot), pozitif yüklü iyonlar ise negatif elektrota (katot) doğru çekilirler. Bir hidrojen iyonu negatif elektroda ulaştığında, burada eksik elektronunu tamamlar ve nötr atom haline gelir. Bu nötr atom gaz kabarcıkları halinde yükselir. Hidrojen iyonu yerine metal iyonu olması halinde, bu iyon da aynen elektrot üzerinde nötr hale geçer. Ancak hidrojen gibi gaz olmadığından elektrot üzerinde birikmeye başlar. Yani elektrot bu metal ile kaplanmaya başlamıştır. Pozitif yüklü iyonlar akım yönünde negatif yüklü iyonlar akım yönünün tersine hareket ederler.
Ayrıca pozitif elektrotta ( anot ) bazı kimyasal olaylar da oluşabilir. Örneğin elektrolitin seyreltilmiş sülfürik asit (H2SO4) olması durumunda, katottan yine hidrojen gazı çıkarken anottan oksijen gazı çıkacaktır. Burada da elektrik akımı suyu elektrolit yardımıyla elemanlarına yani oksijen ve hidrojene ayrıştırmıştır.
Özetle, doğru akım uygulanarak bir elektrolitin elemanlarına ayrıştırma işlemine elektroliz denir.
Açığa çıkan madde miktarının belirlenmesi
Bir elektroliz olayında katotta açığa çıkan maddenin miktarı akım ve zamanla orantılıdır. 1 amperlik bir akım şiddetinde ve 1 saniyede açığa çıkan madde miktarına elektrokimyasal eşdeğer (akuvalans) denilir. Bu akuvalans değeri her bir element için farklıdır.
m = I . t . c m: kütle I : akım t : zaman c : elektrokimyasal eşdeğer
Örnek: 1,5 A bir akım şiddetinde ve 10 dk sürede bir gümüş nitrat eriğinden açığa çıkan gümüşün miktarı nedir?
m = I . t . c = 1,5 . 10 . 60 . 1,118 = 1006,2 mg = 1,0062 gram
Ayrıca 1 amper şiddetinde elektrik akımı 1 saniyede gümüş tuzu eriğinden 1,118 mg gümüş açığa çıkarır tanımı amperin tariflerindendir.
Böylece bu yazımızda da elektrolit ve elektroliz nedir öğrenmiş olduk. Bizleri takipte kalın.

“Elektrolit ve Elektroliz” üzerine bir yorum
Merhaba Bir projede bu tip bir çalışma yaptım elektro yıpranmasına karşı krom ve grafit kullandım fakat aşınmayı durduramadı
En dayanıklı elektrot olarak ne kullanmalıyım yardımınıza ihtiyacım var